B30-24 Aminosäurezusammen-setzungsanalyse in alternativen proteinhaltigen Lebensmitteln
Experimentelle Details
Einleitung
Mit zunehmender Besorgnis um die globale Ernährungssicherheit und die Auswirkungen der traditionellen Tierhaltung auf die Umwelt wächst auch der Markt für alternative Proteine, seien es pflanzliche Proteine, Mykoproteine, aus Insekten gewonnene Proteine oder kultiviertes Fleisch.
Bei der Herstellung alternativer Proteinprodukte für den Markt gibt es zahlreiche Anwendungsbereiche, in denen eine Aminosäureanalyse empfohlen wird. Die wichtigsten Bereiche sind Geschmack(1), Analyse der Qualität und Verdaulichkeit der Proteine(2) und genaue Analyse des Gesamtproteingehalts(3). In dieser Anwendung haben wir die Aminosäureprofile eines Rindfleischburgers einer Supermarktmarke mit denen eines bekannten pflanzlichen Burgers verglichen.
Probenahme
Das Biochrom-Gerät kann genaue Ergebnisse aus Proben im Milligrammbereich oder darunter liefern. Bei der Untersuchung natürlicher Materialien ist es jedoch vorzuziehen, größere Mengen zu verwenden, um Inhomogenitäten in der Probenmatrix zu überwinden. Die Verfügbarkeit von Material ist bei Lebensmitteln selten ein Problem, und das war auch hier nicht der Fall. Daher haben wir für diese Untersuchung 1 g [~1 %] Proben aus den Artikeln entnommen.
Analyseoptionen
Manchmal besteht Interesse daran, freie Aminosäuren in Lebensmitteln zu quantifizieren. Dadurch können auch Zusatzstoffe und Ähnliches identifiziert werden, z. B. Geschmacksverstärker wie Mononatriumglutamat und Aspartam. Dies erfolgt durch Extraktion mit verdünnter Salzsäure. Bei Fleisch und Fleischersatzprodukten liegt die überwiegende Quelle für Aminosäuren natürlich in den Proteinen, so dass in diesem Fall der Extraktionstest nicht anwendbar ist.
Es ist möglich, Proteine durch einfache Hydrolyse mit konzentrierter Säure in ihre Bestandteile zu zerlegen. Leider werden bei diesem Verfahren einige Aminosäuren wie Cystein/Cystin, Methionin und Tryptophan zerstört. Umfassendere Ergebnisse erhält man, wenn man die Proben vor der Hydrolyse oxidiert: Dadurch werden die schwefelhaltigen Aminosäuren in Cysteinsäure und Methioninsulfon umgewandelt, die gegen Säureabbau resistent sind. Wir haben diese Methode angewendet. Tryptophan kann separat durch alkalische Hydrolyse quantifiziert werden. Es gibt mehrere Varianten dieses Verfahrens, und wir haben uns für eine seit langem etablierte Methode unter Verwendung von Bariumhydroxid(4) entschieden.
Verfahren
Die getesteten Produkte wurden über bekannte Einzelhändler bezogen und wurden in Großbritannien hergestellt. Aliquots [1 g] der Fleisch- und Pflanzenburger wurden in 50-ml-Rundkolben überführt. Zu jedem wurden 5 ml Oxidationsreagenz(5) hinzugefügt. Die Kolben wurden über Nacht bei < 4 °C gelagert. Die Proben wurden auf Raumtemperatur erwärmt und vorsichtig mit Natriummetabisulfit [0,84 g] versetzt, um das Oxidationsmittel zu zerstören. Die Kolben wurden mit Wasserkühlern versehen und in ein Heizbad gestellt. Die Kolben wurden mit Hydrolysereagenz [12 ml](6) und einigen Anti-Bumping-Granulaten versetzt und der Inhalt wurde 24 Stunden lang unter leichtem Rückfluss gehalten. Nach Abkühlen auf Raumtemperatur wurde der Inhalt unter Vakuum mit einem Rotationsverdampfer zu einem Film reduziert. Die Rückstände wurden in Ladepuffer(7) aufgenommen und in 50-ml-Messkolben überführt. Es wurde 1 ml interner Standard(8) hinzugefügt und das Volumen mit mehr Puffer bis zur Markierung aufgefüllt.
Die Proben für die Chromatographie [ ~ 0,5 ml] wurden filtriert und in einem Arbeitsgang unter Verwendung von Uniprep-Fläschchen(9) in den Autosampler überführt. Es wurde ein Fläschchen mit gepuffertem Referenzstandard mit geeigneten Aminosäuren und einem internen Standard von 0,5 mM vorbereitet(10). Zur Erstellung einer Blindprobe wurde außerdem ein Fläschchen mit ausschließlich Puffer vorbereitet. Die Chromatographie wurde unter Verwendung des Programms „Sodium Oxidised High Performance” auf dem Ionenaustauschgerät Biochrom 30+ mit geeigneten Puffern durchgeführt.
Für die alkalische Hydrolyse wurden 200 mg Proben zusammen mit 100 mg Stärke, 6 g Bariumhydroxid und 50 ml Wasser in 50-ml-Rundkolben überführt. Die Proben wurden über Nacht unter Rückfluss erhitzt und auf Raumtemperatur abgekühlt. Es wurde ausreichend Salzsäure (konzentriert) hinzugefügt, um das Bariumhydroxid (~3,5 ml) aufzulösen, und das Volumen wurde mit einem Ladepuffer in einem Messkolben auf 50 ml aufgefüllt. Die Proben wurden filtriert und wie zuvor beschrieben analysiert.
Hinweis: Es gab keine offensichtlichen Anzeichen für Fettrückstände in den hydrolysierten Proben: In Fällen, in denen diese in großen Mengen vorhanden sind, ist es ratsam, sie mit einem mit Wasser nicht mischbaren Lösungsmittel wie Leichtbenzin zu extrahieren und zu entsorgen.
Ergebnisse
Die folgenden Chromatogramme [570 nm-Kanal. Schwarz = Standard, rot = Fleisch, grün = pflanzlich] zeigen alle Aminosäuren, die innerhalb von 67 Minuten unter Verwendung eines Standardprogramms vollständig aufgelöst wurden. Cystein und Methionin wurden vollständig in ihre oxidierten Formen umgewandelt, was auf eine ausreichende Penetration des Oxidationsreagenzes in die Probenmatrix hinweist. Asparagin wurde in Asparaginsäure umgewandelt. Die Werte für Hydroxyprolin und Prolin wurden aus dem 440-nm-Kanal entnommen [nicht dargestellt].
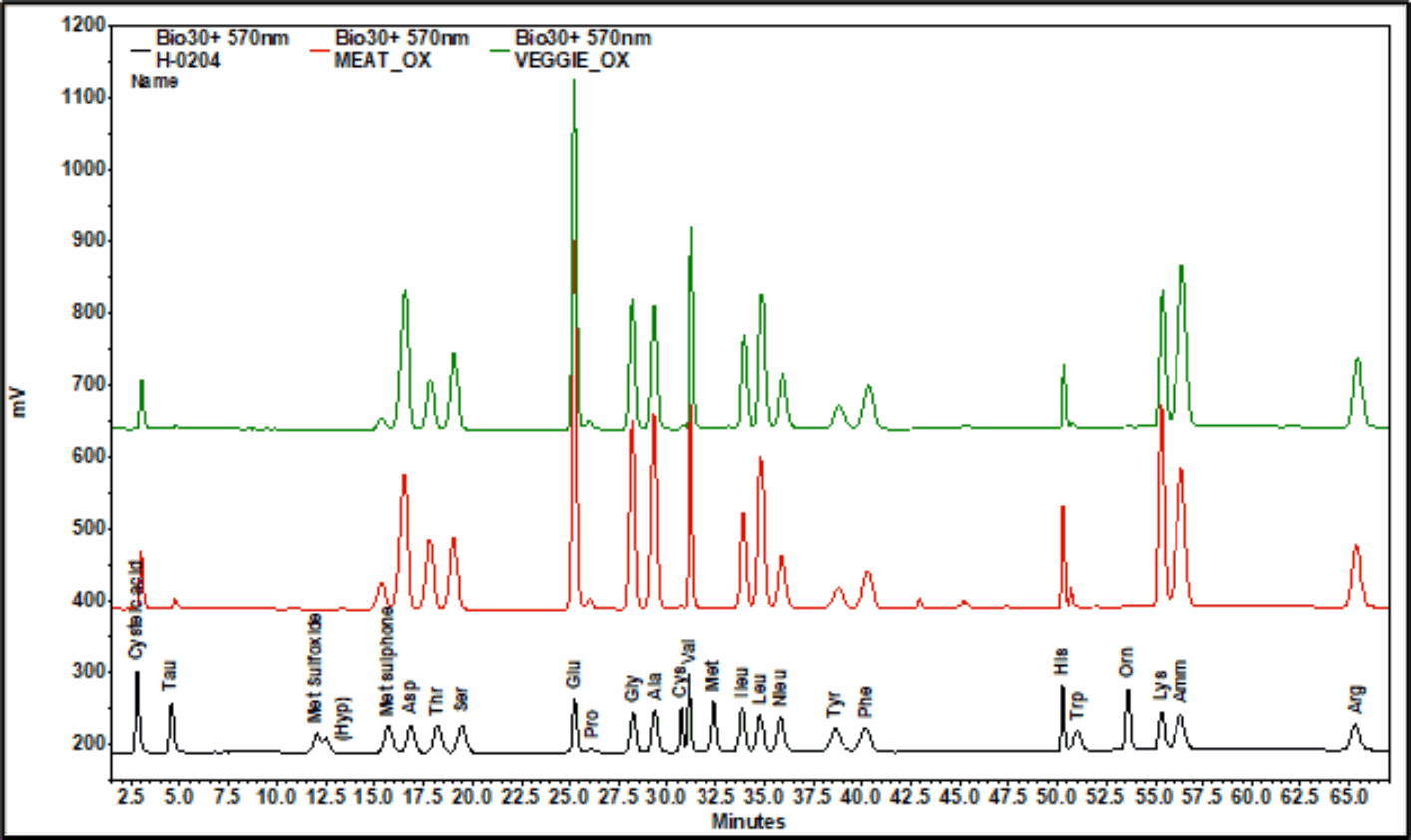
Die Peakflächen wurden unter Verwendung der individuellen Response-Faktoren aus dem Standard in Konzentrationen umgewandelt und sind in der folgenden Tabelle dargestellt.
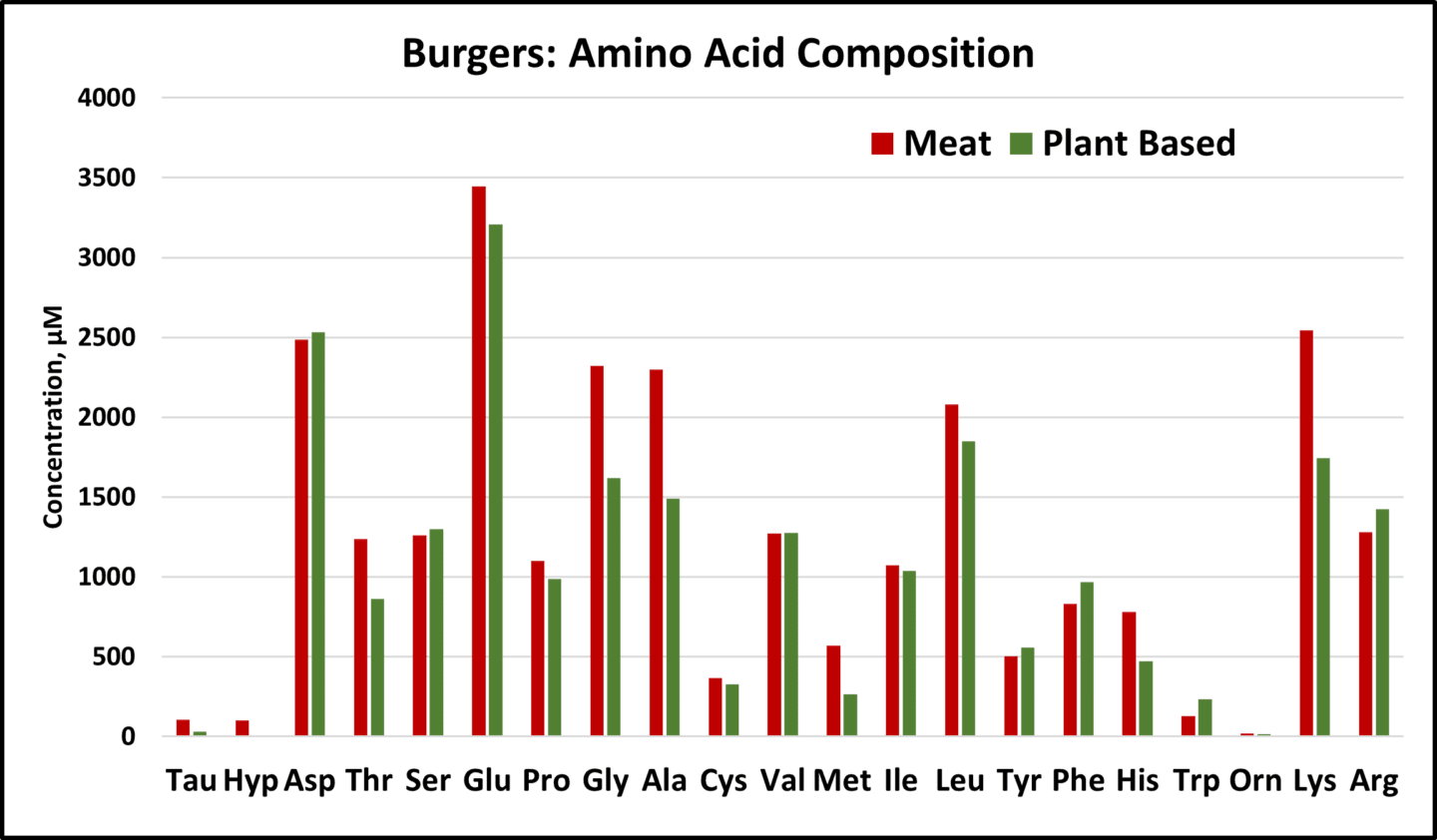
Die beiden Produkte waren in ihrer Zusammensetzung sehr ähnlich, da alle essentiellen Aminosäuren (Thr, Val, Met, Ile, Leu, Phe, His, Trp, Lys) in beiden enthalten waren. Die Konzentrationen von Threonin, Histidin, Methionin und Lysin waren jedoch im Rindfleischprodukt deutlich höher.
Durch einfache Multiplikation der molaren Konzentration jeder vorhandenen Aminosäure mit dem Restmolekulargewicht und anschließender Summierung lässt sich die Proteinzusammensetzung direkt berechnen. Dadurch werden Fehler bei der Verwendung von Ersatzmethoden wie Gesamtstickstoff vermieden. Es wurden Werte von 17 % für Fleischprodukte und 15 % für pflanzliche Produkte ermittelt, die weitgehend mit den auf der Verpackung angegebenen Werten übereinstimmen.
Fazit
Die Aminosäureanalyse mit dem Biochrom Bio 30+ ist eine einfache und hochpräzise Methode zur Trennung und Quantifizierung der Aminosäuren in einer Vielzahl traditioneller und alternativer proteinhaltiger Lebensmittel für den menschlichen Verzehr.
Die Ergebnisse dieser Analyse können in verschiedenen Bereichen der Entwicklung und Herstellung genutzt werden, darunter die Überwachung der Proteinzusammensetzung von Zellkulturen und Medien, die Verfeinerung von Geschmacksprofilen, die Nährwertanalyse für Kennzeichnungszwecke und die Bestimmung der Qualität von wenig anerkannten Bewertungssystemen wie PDCAAS.
Referenzen/Quellen
(1.) Joo ST, Choi JS, Hur SJ, Kim GD, Kim CJ, Lee EY, Bakhsh A, Hwang YH. Eine vergleichende Studie zu den Geschmackseigenschaften von aus Hühner- und Rindermuskeln gewonnenem Fleisch aus Satellitenzellkulturen. Food Sci. Anim. Resour. Januar 2022; 42(1):175-185.
(2.) Amare, E, Mouquet-Rivier, C, Servent, A. , Morel, G. , Adish, A. und Haki, G. Proteinqualität von in Äthiopien angebauten Amaranthkörnern unter dem Einfluss von Poppen und Fermentierung. Food and Nutrition Sciences, 6, 38-48. 2015.
(3.) Mæhre HK, Dalheim L, Edvinsen GK, Elvevoll EO, Jensen I-J. Proteinbestimmung – Die Methode ist entscheidend. Lebensmittel. 2018; 7(1):5.
(4.) A. Dreze und W.S.Reith Biochem. J. 62 (1956) 3P. Auch A. Dreze Bull. Soc. Chim. Biol., 42 (1960) 407
(5.) Bereiten Sie eine Stammlösung aus 45 g Ameisensäure (100 %), 250 mg Phenol und 5 g Wasser vor. Bereiten Sie das Oxidationsreagenz unmittelbar vor Gebrauch zu, indem Sie 18 ml der oben genannten Stammlösung mit 2 ml wässrigem Wasserstoffperoxid (30 %) mischen und 1 Stunde lang bei Raumtemperatur rühren. Vor Gebrauch auf unter 4 °C kühlen.
(6.) Das Hydrolysereagenz wird aus 50 ml konzentrierter Salzsäure und 100 mg Phenol hergestellt, das mit Wasser auf 100 ml aufgefüllt wird.
(7.) Biochrom-Natrium-Ladepuffer #80-2037- 57
(8.) Interne Standard-Stammlösung, 2 mM, hergestellt aus 131 mg Norleucin in 50 ml Ladepuffer.
(9.) Mini-UniPrep-PVDF-Filter, 0,2 µm. Cytiva [Whatman].
(10.) Ein Arbeitsreferenzstandard wurde aus 1 Teil Biochrom Protein Oxidised Standard 2,5 mM, #80-6002-68, 1 Teil Norleucin 2,5 mM und 3 Teilen Ladepuffer hergestellt.
Quelle: Application B30-24 Amino Acid Analysis for Alternative Protein Products (2022) Biochrom Ltd., Cambridge, Großbritannien
Ein Auszug dieses Artikels wurde im Nov. 2025 auch in der Laborfachzeitschrift LABO veröffentlicht, Link zum Beitrag: Aminosäureanalyse: Proteingehalt und Proteinqualität von Fleisch vs. Fleischersatz - LABO

Sprechen Sie mit uns über Ihre Anforderungen
Wir nehmen uns Zeit für Ihre Situation. Welche Proben analysieren Sie? Wie viele pro Woche? Welche Anforderungen haben Sie an Reproduzierbarkeit und Verfügbarkeit? In einem Gespräch klären wir, ob das Biochrom B30Plus zu Ihren Workflows passt – und wie wir Sie langfristig unterstützen können. Unverbindlich, konkret, auf Augenhöhe.

Funktioniert. Seit 25+ Jahren.

Jahre am Markt

Aller Ausfälle am Telefon behoben

Reaktionszeit

Akteure für 8 Länder



